Карбонатность
Нормативная документация: ГОСТ 34467-2018
Введение
Карбонатные компоненты в грунтах (кальцит, доломит, сидерит и др.) существенно влияют на их инженерно-геологические свойства, включая растворимость, несущую способность и устойчивость к химической агрессии. Наличие карбонатов, особенно кальцита (CaCO3), определяет риски карстообразования, суффозии и коррозии строительных конструкций. Содержание этих соединений выражается в процентах CaCO3 или CO2 от массы абсолютно сухого грунта. Настоящая статья описывает методы определения карбонатности по ГОСТ 34467-2018 и один альтернативный метод (Метод В.Е. Соколовича)
Рассматриваются:
- Гравиметрический метод (по потере массы),
- Манометрический метод (по давлению CO2),
- Метод титрования (Метод В.Е. Соколовича)
Гравиметрический метод (PS_GRAV)
1.1 Краткое описание
Применяется для точного определения массовой доли карбонатов во всех типах минеральных грунтов. Основан на химическом разложении карбонатов соляной кислотой с последующим измерением массы нерастворимого остатка.
1.2 Вычисляемые параметры:
- Относительное содержание CO₂ в грунте (д.е.)
- Относительное содержание CaCO₃ в грунте (д.е.)
1.3 Теоретические основы
Карбонаты (CaCO₃, MgCO₃) реагируют с соляной кислотой:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
Массовая доля карбонатов рассчитывается по потере массы образца после реакции.
Методика
-
Подготовка пробы:
Отбирают навеску грунта массой 15-20 г для параллельного определения гигроскопической влажности по ГОСТ 5180. -
Подготовка оборудования:
В химический стакан (100-250 мл) наливают 20 мл 5н раствора HCl (готовится по Приложению Б ГОСТ).
Накрывают стакан часовым стеклом, на которое устанавливают пустой фарфоровый тигель. -
Первое взвешивание:
Взвешивают систему (стакан + HCl + часовое стекло + тигель) с точностью ±0.01 г → P₁. -
Второе взвешивание:
Помещают в тигель аналитическую навеску грунта 3-5 г.
Повторно взвешивают всю систему → P₂. -
Проведение реакции:
Тигель с навеской осторожно погружают в HCl, избегая разбрызгивания.
Накрывают часовым стеклом, аккуратно перемешивают круговыми движениями до прекращения вскипания.
Выдерживают 30 минут. -
Третье взвешивание:
Взвешивают систему после реакции → P₃.
Расчеты
- Относительное содержание CO₂ (д.е.):
CO₂ = [ (P₂ - P₃) / (P₂ - P₁) ] × 100%
Где:
P₂ - P₃ = масса выделившегося CO₂ (г)
P₂ - P₁ = масса анализируемой навески (г)
- Относительное содержание CaCO₃ (д.е.):
CaCO₃ = CO₂ / 0.44
Где 0.44 - коэффициент, учитывающий атомную массу СО2
Манометрический метод (PS_MANO)
2.1 Краткое описание
Используется для быстрого определения содержания карбонатов путем измерения давления CO₂ в герметичном кальциметре .
2.2 Вычисляемый параметр:
- Содержание CaCO₃ в грунте (г)
2.3 Теоретические основы
Объем выделившегося CO₂ пропорционален количеству карбонатов в исходном грунте. Давление газа измеряется манометром и пересчитывается в массу CaCO₃.
Методика
Принцип работы кальциметра:
Измерение давления CO₂, выделяющегося при реакции карбонатов грунта с соляной кислотой в герметичном реакционном цилиндре (кальциметре). Давление пропорционально содержанию CaCO₃.
Этапы проведения испытания:
- Подготовка прибора (калибровка):
- Строят калибровочную кривую по чистому CaCO₃:
- Готовят 5 серий навесок: 0.2 г, 0.4 г, 0.6 г, 0.8 г, 1.0 г (±0.01 г)
- Для каждой навески измеряют давление после реакции с HCl
- Строят график "Масса CaCO₃ → Давление" (Приложение Г ГОСТ)
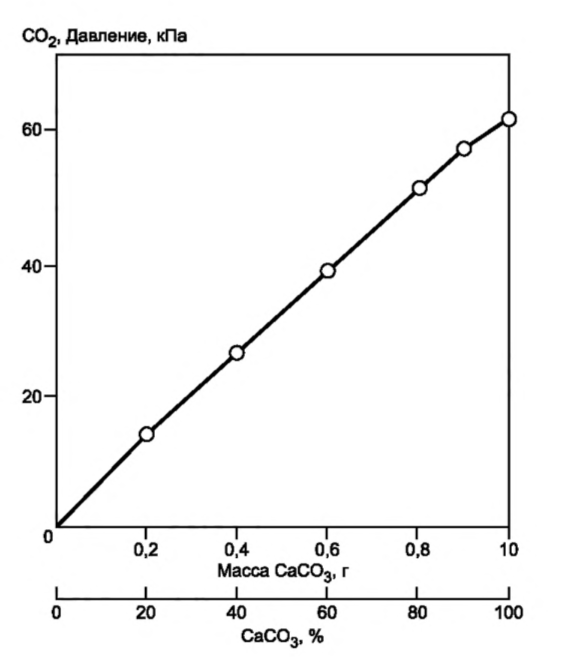
Рис. 1 Приложение Г. Калибровочная кривая кальциметра ГОСТ 34467—2018
-
Подготовка пробы:
- Берут воздушно-сухой образец массой 1.0 г
- Помещают в чашку реакционного цилиндра
-
Проведение реакции:
- В цилиндр наливают 20 мл 1н HCl
- Устанавливают чашку с пробой (рис. В.1 ГОСТ)
- Герметично закрывают цилиндр с уплотнительными кольцами
- Наклоняют и вращают цилиндр для смешивания пробы с кислотой
-
Измерение давления:
- Через 5 мин после начала реакции фиксируют максимальное давление по манометру
- Открывают предохранительный клапан для сброса давления
-
Очистка системы:
- Сливают содержимое
- Промывают цилиндр и чашку дистиллированной водой
Расчет
- По калибровочной кривой определяют массу CaCO₃ (г), соответствующую измеренному давлению
Масса CaCO₃ = f(ΔP)
Где f - функция калибровочной кривой
- Для ориентировочной оценки используют таблицу А.1 ГОСТ:
Метод титрования 1н. раствором HCl (PS_TITR)
3.1 Краткое описание
Экспресс-метод для определения карбонатности грунтов через косвенное титрование. Основан на преобразовании карбонатов в растворимый карбонат натрия с последующим кислотным титрованием.
3.2 Вычисляемые параметры:
- Относительное содержание CO₂ (д.е.)
- Относительное содержание CaCO₃ (д.е.)
3.3 Теоретические основы
1. Карбонаты преобразуются фторидом натрия:
CaCO3 + 2NaF → CaF2↓ + Na2CO3
-
Образовавшийся Na₂CO₃ титруют HCl:
Na2CO3 + HCl → NaHCO3 + NaCl -
1 мл 1н HCl эквивалентен:
- 0.044 г CO₂
- 0.100 г CaCO₃
Методика
-
Подготовка пробы:
- Воздушно-сухой грунт измельчают и просеивают через сито 0.25 мм
- Отбирают навеску 4-5 г (±0.001 г)
-
Предварительная нейтрализация:
- Пробу помещают в колбу с 80 мл дистиллированной воды
- Добавляют 3-5 капель фенолфталеина
- Если появляется розовая окраска (щелочность), титруют 0.5н HCl до обесцвечивания
-
Основная реакция:
- Добавляют 4 г кристаллического NaF
- Кипятят 5 мин
- Охлаждают до 20-25°C
-
Титрование:
- Добавляют новые 3-5 капель фенолфталеина
- Титруют 1н HCl до исчезновения розовой окраски
- Фиксируют объем кислоты (a, мл)
Расчетные формулы:
CO2 = (a × 0.044 × 100) / m
CaCO3 = (a × 0.100 × 100) / m
где:
- a — объем 1н HCl на титрование (мл)
- m — масса сухого грунта (г)
- 0.044 — масса CO₂, эквивалентная 1 мл HCl (г)
- 0.100 — масса CaCO₃, эквивалентная 1 мл HCl (г)